1 вид. Дана масса раствора продукта или одного из исходных веществ реакции. Вычислить массу (объем) исходного вещества или продукта реакции.
1 действие: вычисляем массу продукта или одного из исходных веществ реакции
2 действие: вычисляем массу или объем исходного вещества по алгоритму.
Пример задачи: К раствору
хлорида алюминия массой 53,2 г и массовой долей 5% прилили избыток раствора
нитрата серебра. Вычислите массу образовавшегося осадка.
Разбор
решения.
Задача ля самостоятельного
решения.
1.Через раствор гидроксида кальция пропустили углекислый газ. Образовалось 324 г раствора гидрокарбоната кальция с массовой долей 1%. Вычислите объём прореагировавшего газа.
2 вид. Дана масса раствора вещества или продукта реакции. Вычислить массовую
долю вещества или продукта реакции.
1 действие: по алгоритму вычисляем массу исходного
вещества (продукта) реакции. На массу
его раствора не обращаем внимания.
2 действие: Знаем массу исходного вещества (продукта)
- нашли в первом действии. Знаем массу раствора – дана в условии.
Находим массовую долю.
Пример задачи: 73 г раствора соляной кислоты смешали с порцией карбоната кальция. При
этом выделилось 0,896 л газа. Вычислите массовую долю исходного раствора соляной кислоты.
Разбор
решения
Задача для самостоятельного решения.
1. К 200 г раствора хлорида кальция добавляли раствор карбоната натрия до прекращения выпадения осадка. Масса осадка составила 12,0 г. Рассчитайте массовую долю хлорида кальция в исходном растворе. (Относительную атомную массу хлора примите равной 35,5)
3
тип. Дана
массовая доля раствора исходного вещества. Определить массу исходного вещества.
1 Действие.
По алгоритму найти массу исходного вещества.
2 Действие. Знаем массу исходного вещества (по
первому действию). Знаем массовую долю (из условия). Находим
массу раствора.
Пример
задачи: к раствору карбоната калия с массовой долей 6% добавили избыток раствора
хлорида бария. В результате образовался осадок массой 9,85г. Определите массу
исходного раствора карбоната калия.
Разбор
решения
Алгоритм
Задача №1
К
Шаблон решения задачи
|
Шаги
алгоритма задачи |
Оформление |
|
1)Для
того чтобы решить задачу для начала нужно написать дано.
|
Дано: m(CuCl2) = w(CuCl2) = 10% = 0.1 Найти: m (CuS) =? |
|
2)
После написания дано, пишем уравнение реакции:
|
CuCl2 + Na2S → CuS↓ + 2Nacl CuS – это осадок (или по-другому – нерастворимое вещество) Мы это узнаем по таблице растворимости, и его нам надо найти. |
|
3) Обязательно надо
запомнить, что после написания уравнения реакции надо уравнять (или поставить коэффициенты около соединений,
где нужно, иначе у вас не сойдется с ответом). |
|
|
4) Рассчитываем массу
и количество вещества хлорида меди (II) содержащегося в растворе:
|
m(чистого вещества) =
m(вещества) m(CuCl2) = v (вещества) = m\М; M – молярная масса, v(CuCl2) = 2.7г/135г\моль = 0,02 моль |
|
5) Откуда найти
молярную массу вещества?
|
Ее можно посмотреть в
таблице Менделеева. Она стоит между элементом и названием элемента, посередине. M(Cu) = 64 г/моль, а M(Cl) = 35.5 г/моль. Но в
задаче дано M(Cl2) = 35.5 При решении задач не забывайте молярные массы округлять до целых. Молярные массы
складываем M (Cu) + M(Cl2) = 64 + 71 = 135 г/моль M(CuCl2) |
|
6) Всегда пишите к каждому числу единицу измерения. Если единицы
измерения повторяются, то их смело можно зачеркнуть. |
У количества вещества единица измерения измеряется в молях. У массы
вещества в килограммах, граммах и тоннах. У молярных масс в кг/моль и г/моль. |
|
7) Определяем массу
вещества, выпавшего в осадок.
|
а) По уравнению
реакции надо сравнить количество (CuCl2) и (CuS) 1 : 1 – это соотношение двух веществ Это значит, что
количество (CuCl2) взято такое же, как и у CuS и оно равно 0.02 молям. б) Находим массу
осадка. Она находится по формуле: m (вещества) = v |
1.К раствору сульфата алюминия массой 68,4 г и массовой долей 8% прилили
избыток раствора хлорида бария. Вычислите массу образовавшегося
осадка.
2. Вычислите объём
газа (н. у.), который выделится при действии избытка сульфида железа(II)
на 490 г 10%-ного раствора серной кислоты.
1. ВЕЩЕСТВА
Периодическая система элементов и строение атома
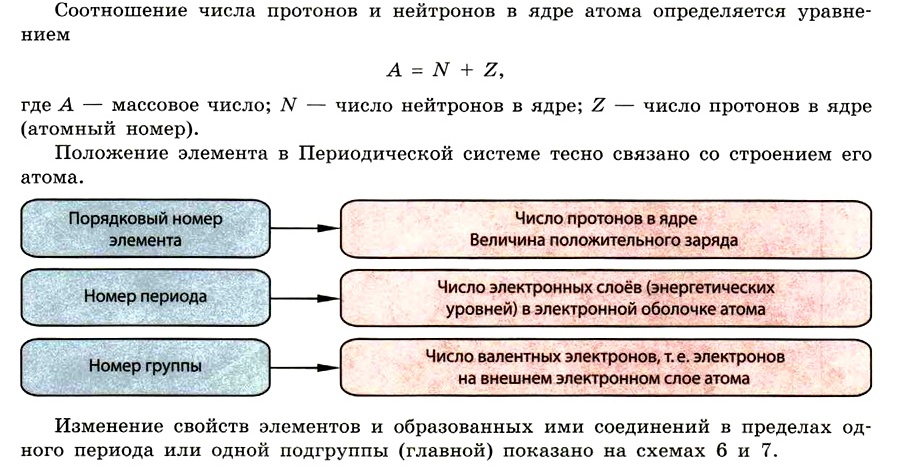
Основные классы неорганических веществ
2. ХИМИЧЕСКИЕ РЕАКЦИИ
Классификация химических реакций
Химические реакции следует отличать от физических явлений. При химических реакциях происходит превращение одних веществ в другие, в то время как при физических явлениях состав веществ не претерпевает изменений.
Признаками химических реакций могут служить:
- изменение цвета;
- выпадение осадка;
- выделение газа;
- изменение окраски индикатора;
- появление запаха и др.
Следует помнить, что ни один из перечисленных признаков не гарантирует протекание химической реакции, а лишь указывает на возможное её осуществление.
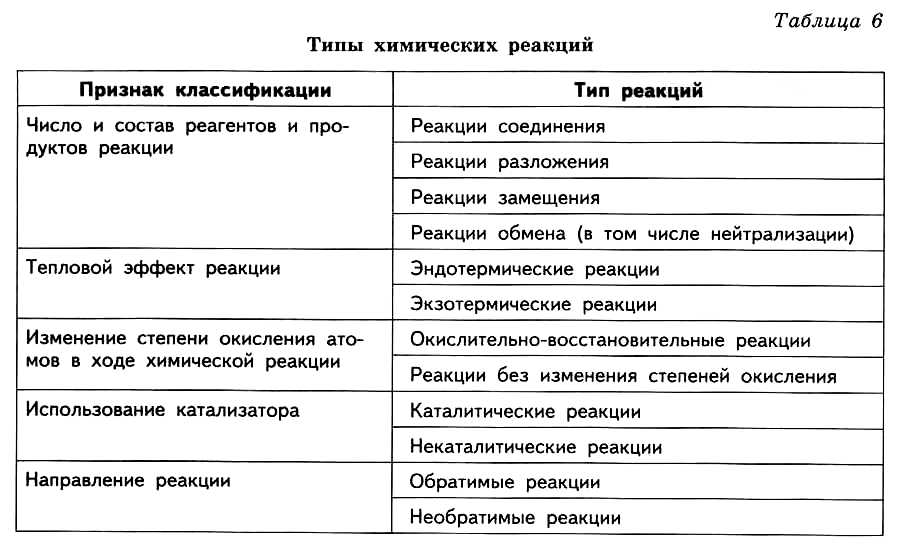
Классификация химических реакций по различным признакам приведена в таблице 6.
Электролиты и неэлектролиты.
Электролитическая диссоциация


Реакции ионного обмена
Протекание реакций обмена с участием электролитов в растворах (реакции ионного обмена) возможно при соблюдении одного из условий (правило Бертолле):
- выпадение осадка;
- выделение газа;
- образование слабого электролита (в частности, воды).
Противоположно заряженные ионы, которые при соединении образуют малорастворимое вещество, газ или молекулы слабого электролита, совместно существовать в растворе без взаимодействия не могут.
Окислительно-восстановительные реакции
3. ОСНОВЫ НЕОРГАНИЧЕСКОЙ ХИМИИ
Химические свойства простых веществ
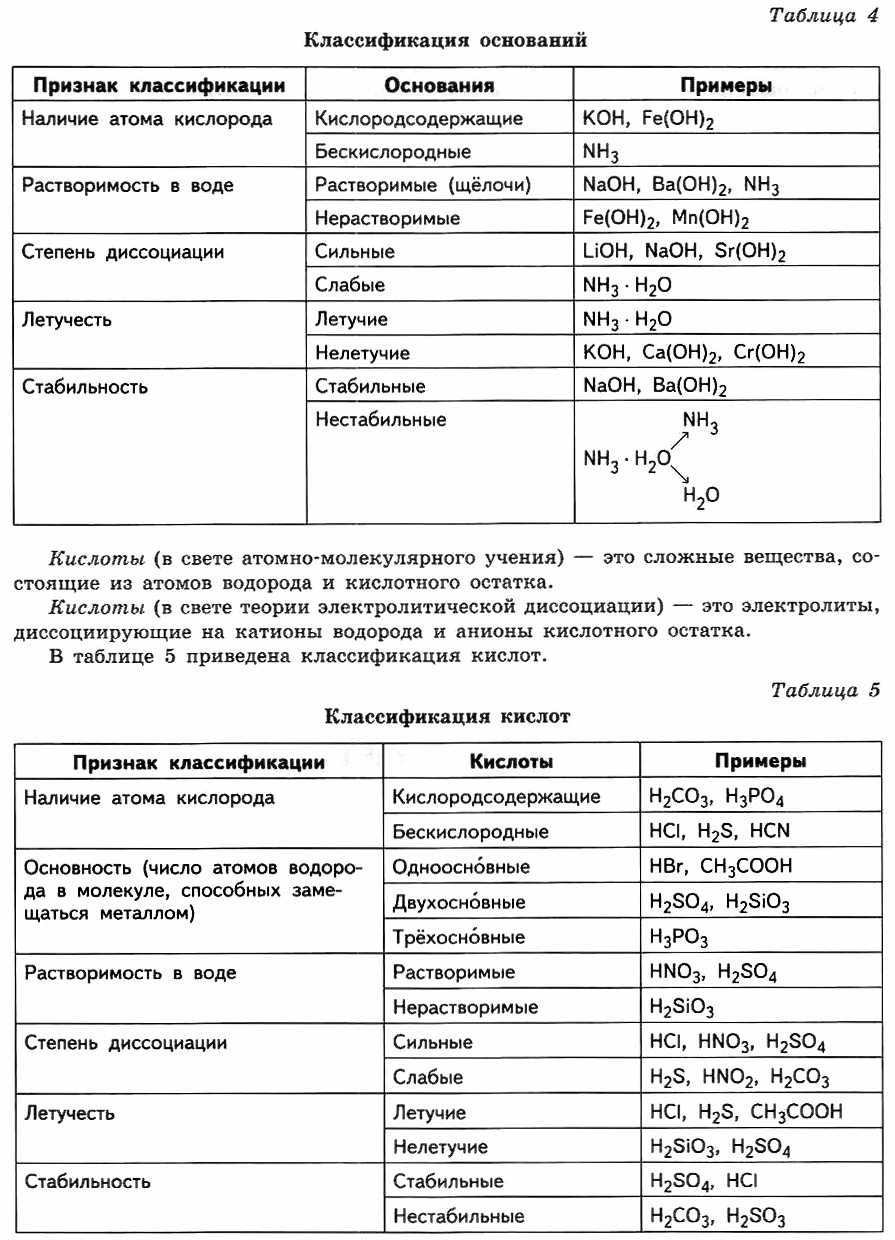
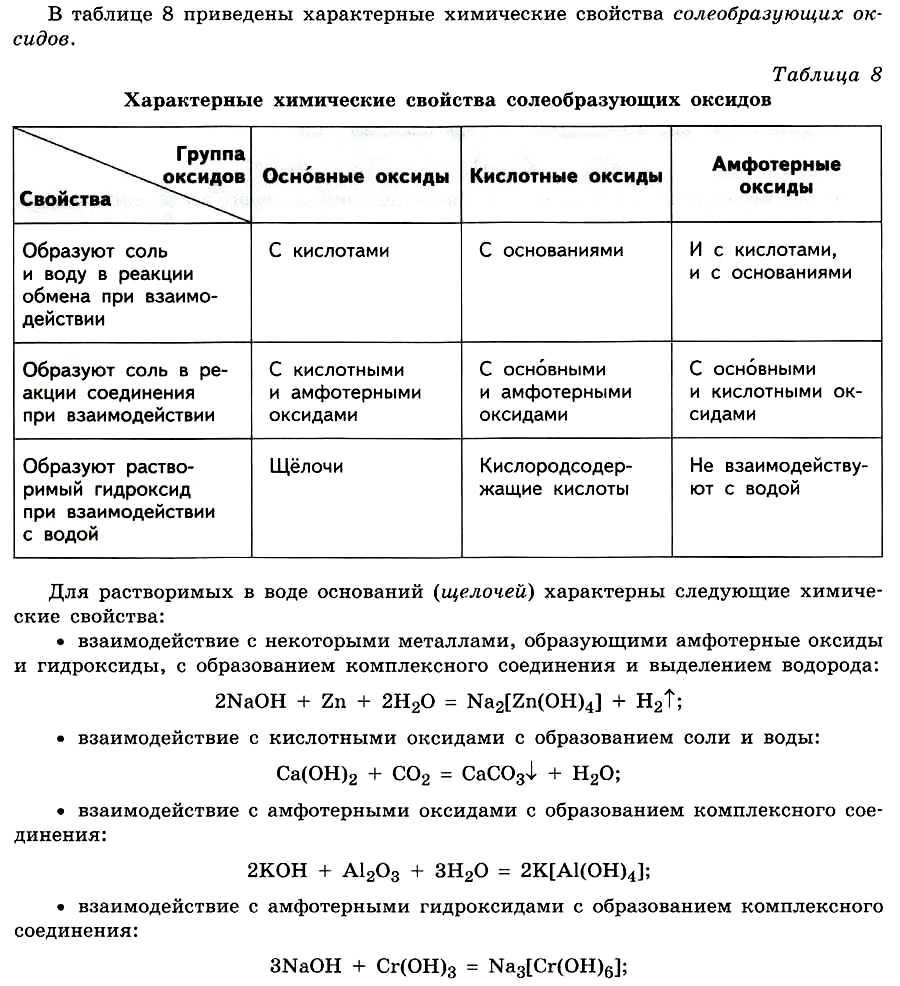
Химические свойства сложных веществ
4. МЕТОДЫ ПОЗНАНИЯ ВЕЩЕСТВ И ХИМИЧЕСКИХ РЕАКЦИЙ
Определение кислотности среды с помощью индикаторов
Качественные реакции в неорганической химии

Получение неорганических веществ




















Комментариев нет:
Отправить комментарий